


时间地点
组织单位
药视网
徐州易云企业服务有限公司
蒲公英、药视网、制药台、药聘网
课程内容
课程一、FDA关于批准前检查要点
1.指南修订历史
2.批准前检查指南适用范围
二、批准前检查策略及
三、批准前检查目标及各目标检查重点及实施要求
1.商业化生产的准备目标
a)检查重点
b)实施要求
2.与申请的符合性的目标
a)检查重点
b)实施要求
3.数据可靠性审计的目标
a)检查重点
b)实施要求
4.药品研发质量承诺的目标
a)检查重点
b)实施要求
四、检查报告及监管/行政策略
1.检查报告
2.监管/行政策略
a)暂不批准建议典型问题
课程二、FDA关于生产检查要点及典型问题
1.药品生产检查指南修订历史
2.各剂型检查指南概况
3.检查策略
4.生产检查分类
a)全面检查
b)简化检查
二、六大系统检查要点
1.质量系统
2.设施设备系统
3.物料系统
4.生产系统
5.包装和贴签系统
6.实验室系统
三、六大系统检查典型缺陷项
课程三、FDA483缺陷项分析
二、六大系统中483情况分析
1.质量系统
2.设施设备系统
3.物料系统
4.生产系统
5.包装和贴签系统
6.实验室系统
三、FDA483缺陷项回复分享
课程四、FDA警告信分析
一、近期警告信分析
二、六大系统中典型警告信分析
1.质量系统
2.设施设备系统
3.物料系统
4.生产系统
5.包装和贴签系统
6.实验室系统
三、数据完整性相关典型警告信
课程五、答疑
讲师介绍
讲师:赵老师 资深生产管理专家和GMP高级咨询顾问,从事制药行业工作二十年,生产管理工作十五年以上。熟悉制药企业质量控制相关法规指南等知识体系。专注于生产管理技术人员和员工操作技术培训, 擅长生产管理系统问题诊断。负责过多家制药企业的质量体系及验证项目的项目管理,涉及疫苗、生物制剂、无菌制剂、固体制剂和原料药等多产品、多剂型,标准涉及SFDA、FDA、欧盟等。
培训模式
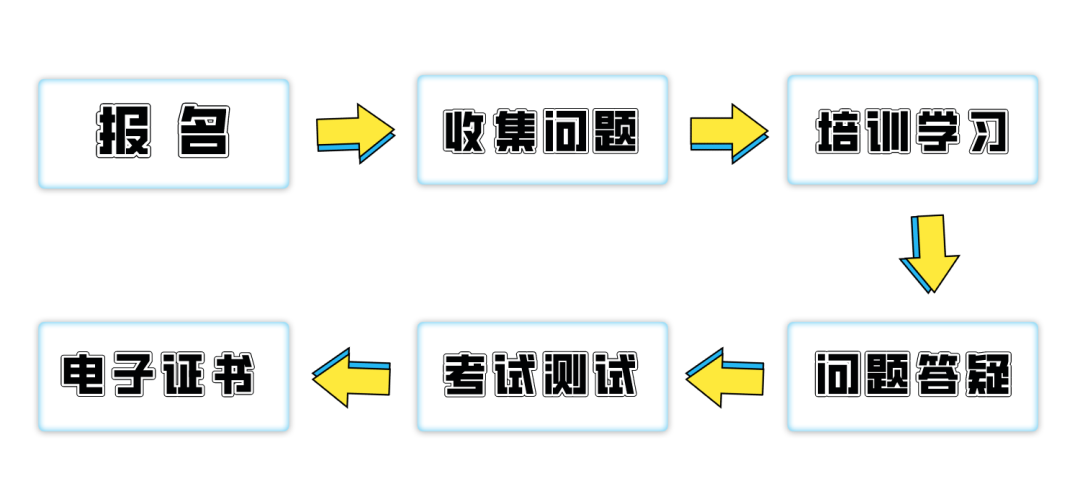
培训特点
1、更专业,更贴心
培训侧重答疑,在培训开始前请各参会企业务必向会务组提交在员工间收集的问题,会务组会和讲师接洽协商,将企业提供的问题融入到课程之中,并且会最大程度的延长答疑时间,以期帮助员工最大程度的解决日常工作中遇到的问题。
2、更方便,更高效
只需要一间会议室+一套投影设备,参会企业可以组织员工一起学习,培训过程中可以同公司同事边交流边学习,培训效果也会更好。
1家企业只需要买1个直播间账号,1个人线下培训的成本可以让n个人接受培训。
去外地参加培训,会有将近一半的时间浪费在路上,旅途的奔波也很辛苦,网络讲堂会使我们节省时间免受旅途奔波的辛苦。

部分企业网络学习展示



费用说明
1、A类票:3500元/端口(含药视网年度VIP/授课费/发票)
2、B类票:2800元/端口(含授课费/发票)
3、药视网年度VIP:500元/端口(含授课费/发票)
4、药视网企业VIP:提供一个免费端口
户名:徐州易云企业服务有限公司
开户行:中国工商银行股份有限公司徐州淮东支行
账号:1106020409210313389
(付款请注明“警告信”)

报名咨询
VIP权益
2、年度VIP有效期内可优惠参与药视网线上直播答疑课(全年约5场)
3、年度VIP有效期内可优惠参与药视网举办的线下培训班(不低于8场)
4、药视网企业VIP有效期内可免费使用药视网培训考试系统

详情咨询
| 文件名 | 上传时间 | 大小 |
|---|