

为帮助各相关企业进一步加强对法规指南的理解,更好的建立有效的污染控制策略,药视网特邀请具有成功实践经验的业内专家共同策划本期学习营,欢迎各相关企业及从业药友报名参与。
培训介绍
开班时间:2024年2月5日
培训时间:2024年2月5日-3月18日
培训地点:药视网培训考试系统
培训对象:药品企业质量管理人员、研发、工程、实验室、验证、微生物管理、微生物检验、医院和科研相关部门人员。
培训内容
一、EU GMP附录1对CCS的法规要求
1、定义:污染与污染控制策略
2、污染控制策略(CCS)的开发 - 目标、模块与管理
3、不同章节中的CCS相关内容
1、建立CCS的基石
① 科学知识
② QRM方法
③ 人员意识
2、工艺设计、微生物控制与监测
① 低生物负荷量产品
② 无菌产品
③ 非无菌产品
3、厂房设施
① 厂房设计
② 人流设计
③ 物流设计
④ 清洁消毒
4、公用系统
① 设计、控制与验证
② HVAC/水系统/工艺用气系统
③ 纯蒸汽系统
5、物料管理
① 质量标准
② 生物污染风险控制
③ 供应商审计
④ 转运/存储/取样风险控制
⑤ 生物药与前沿药物的物料关注
6、环境控制、验证与监测
① 基本原理
② EMPQ – 环境再确认与关键参数
③ 停机与恢复
7、人员管理
① 培训内容
② 人员卫生与更衣
③ 洁净室行为
④ 无菌监督与指导
8、设备管理
① 设计和清洁验证
② 持续控制
③ 特殊关注 – 一次性系统、隔离器、屏障系统、产品通路
④ 维修
9、容器密封系统
① 目标
② 方法开发与验证
10、质量体系
① 质量量度与趋势分析
② 偏差与CAPA
③ 变更
④ 质量风险管理
⑤ 微生物实验室管理
11、CCS的管理与有效性审核
1、差距分析
2、ECA文件模板简介
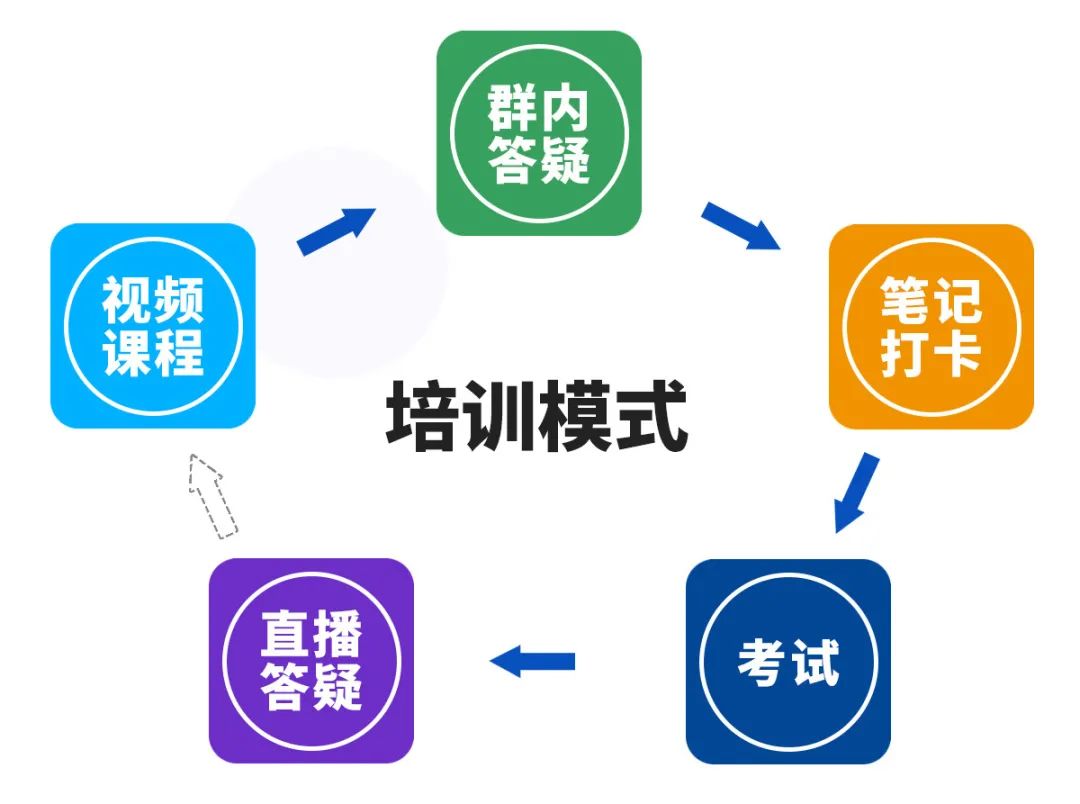
培训模式
包含约35学时课程+4次答疑课+3位讲师+每日群内互动
讲师介绍
叶老师 药视网特聘讲师、ISPE会员,从事无菌制剂、非无菌制剂质量管理20年,欧美认证13年。全面参与原料药、无菌原料药、冻干粉针、小容量注射剂、口服制剂的中国、FDA及欧盟GMP认证工作。对于原料药、无菌原料药及无菌制剂的GMP要求及技术有深入的研究。精通无菌工艺、实验室要求、产品验证、制药用水等。
赵老师 13年无菌药品质量及验证管理经验,丰富的小容量注射剂、大容量注射剂、生物制品、细胞治疗产品质量管理经验,对产品及设备的灭菌工艺及验证、生产过程数据完整性、无菌药品质量监管有非常深入的研究与理解,多次经历FDA cGMP认证与欧盟GMP认证及审计,同时拥有丰富的无菌药品生产车间建设项目经验。
费用说明
1、培训原价:1999元/人(含授课费/证书费/发票)
户名:徐州易云企业服务有限公司
开户行:中国工商银行股份有限公司徐州淮东支行
账号:1106020409210313389
(付款请注明“CCS第二期”)
咨询报名
扫描识别下方二维码进行报名咨询

报名及VIP咨询
| 文件名 | 上传时间 | 大小 |
|---|