

随着药品管理法等法规的不断更新及GMP符合性检查形式的实施,药企需要转变观念,从被动的符合GMP要求转变为主动、持续地管控药品质量风险。
为帮助企业提升验证管理水平,提高验证管理人员的理论和实践能力,更加细致规范的开展验证管理工作,使关键设施、设备、系统、工艺等验证状态的维护更加科学,最终实现更高层次的GMP管理水平,药视网再次联合10位具有多年一线工作经验的讲师推出《GMP验证管理精英训练营(第六期)》
时 间 地 点
Time and place
培训时间:2023年2月21日-2023年4月11日(50天)
培训地点:线上培训
培 训 内 容
Training content
主要内容:
共计:约55学时(按50分钟/学时计)
培 训 模 式
Training mode
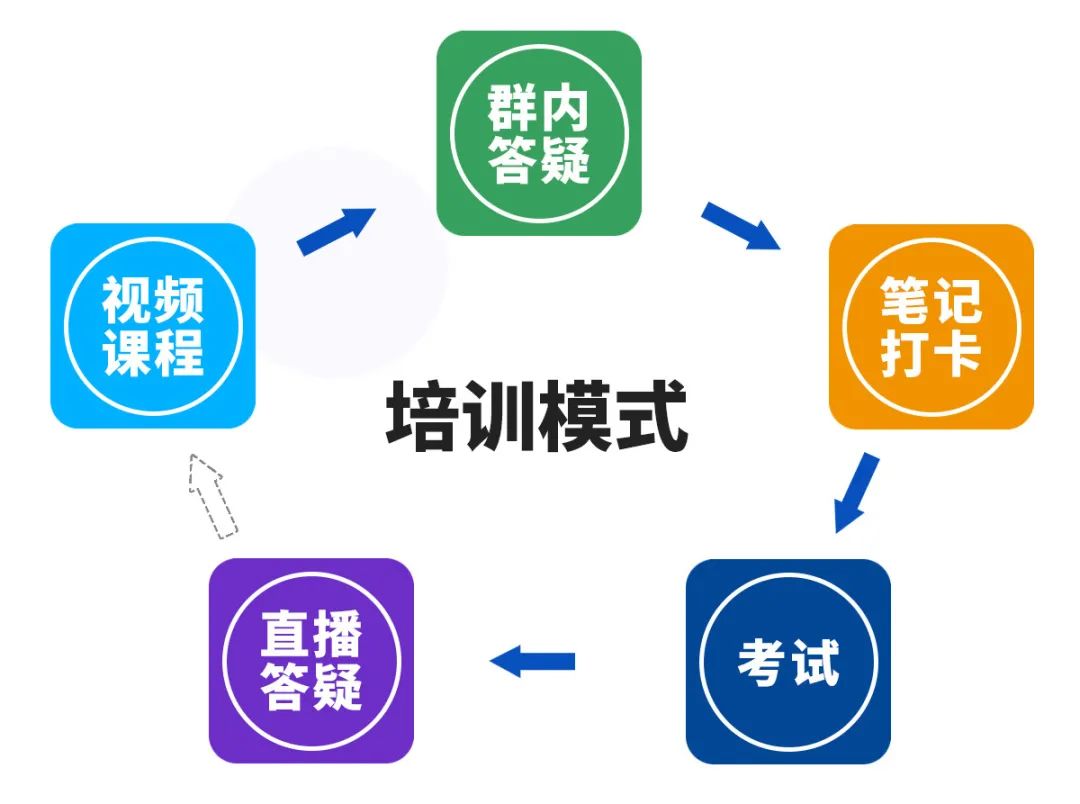
包含约55学时课程+10次答疑课+10位老师讲解+每日群内互动
特别提醒:不是每天都是老师讲课,但是有问题随时可以问,间隔直播答疑。
讲 师 介 绍
Introduction of lecturer
朱老师,主讲嘉宾
先后在国内知名药企从事药品质量管理,药品研发注册工作24年,长期担任公司质量负责人;熟悉中药、化学药各类剂型的技术管理要求,多次领导公司通过GMP认证检查、药品注册检查,具有丰富的药品质量管理、实验室管理经验。
焦红江,空压&空调系统验证
资深专家讲师,蒲公英联合创始人,在国内多家知名药企从事生产管理/设备管理/工程管理、制药工程前期设计、新药厂项目建设管理近30年,具有丰富的GMP实施、GEP管理、制药工程设计、硬件疑难问题解决、厂房设施设备系统的
认验证、预防性维护、计量校准、计算机化系统验证……等经验,熟悉各种制药装备、生产工艺与自动化控制。先后参与或负责过10多个车间的GMP改造、多个FDA、欧盟cGMP认证项目,做过数百个车间的平面图纸审核、工艺概念设计、多家企业内训、现场模拟审计工作。现为自由职业,从事制药项目GEP/GMP咨询、培训、工程设计辅导、项目总包管理、新厂建设辅导、确认与验证外包服务。
占小兵,实验室仪器及分析方法验证
药视网特聘讲师,2004年毕业于南昌大学药学院,从事药品研发分析工作十余年,具有丰富的分析方法开发与验证工作经验,在业内知名公众号发表具有广泛影响力的分析专业方面的文章近百篇,好评如潮。
章老师,微生物检验方法验证
国内某大型医药集团培训讲师,从事制药行业微生物及公用系统检测、动物实验等工作近20年,曾多次参与组建微生物实验室,接受过多次国内外官方审计,负责为公司集团内提供技术支持,具有丰富的实践和管理经验。
胡大伟,计算机化系统验证
国际制药项目管理协会(IPPM)特聘讲师,药视网特聘讲师,曾在香港供职于甲方药企GSK、Fortune及澳美制药,也曾供职乙方IT咨询公司,2019年回到深圳信立泰工作;曾参与ERP,MES,WMS,CDS,PIC/S迎检,欧盟迎检,FDA OCT迎检等项目,有着丰富的计算机化系统验证与数据可靠性合规经验。
叶非,环境消毒验证
蒲公英特聘讲师、ISPE会员,从事无菌制剂、非无菌制剂质量管理20年,欧美认证13年。全面参与原料药、无菌原料药、冻干粉针、小容量注射剂、口服制剂的中国、FDA及欧盟GMP认证工作。所服务的公司,均顺利通过了WHO、FDA、欧盟认证无菌制剂及原料药认证。擅长质量体系的建设、验证和现场的GMP检查。对于原料药、无菌原料药及无菌制剂的GMP要求及技术有深入的研究。精通质量体系建设、实验室要求、无菌工艺、产品验证等。
王兴来,清洁验证
蒲公英论坛知名版主,从业12年,先后从事过化学原料药、血液制品及口服制剂等行业生产、质量管理工作,历任技术研发员、质检员、技术主任等岗位,经验丰富。先后独立组织通过多次新版GMP认证及整改工作,擅长体系建设与维护、工艺技术问题等,尤其擅长运用风险评估的方法合理开展验证与确认工作。
彭老师,计量与校准
某大型药企计量负责人,工程师,国家首批一级注册计量师,参与多家计量建标和校准实验室CNAS认可活动。从事一线计量工作15年,有着丰富的计量校准/管理经验,曾受邀担任当地质检部门举办的企业计量管理人员培训讲师,帮助企业了解计量专业基础知识,提升计量专业管理水平。在制药行业从事计量工作12年,数十次经历注册检查、GMP检查等,建立计量管理体系,内校标准、计量测试技术、分析总结计量管理风险点。
赵高峰,无菌工艺验证
13年无菌药品质量及验证管理经验,丰富的小容量注射剂、大容量注射剂、生物制品、细胞治疗产品质量管理经验,对产品及设备的灭菌工艺及验证、生产过程数据完整性、无菌药品质量监管有非常深入的研究与理解,多次经历FDA cGMP认证与欧盟GMP认证及审计,同时拥有丰富的无菌药品生产车间建设项目经验。
贾老师,仪器验证
8年新药研发质量检验工作经验,7年化药厂、疫苗厂质量控制(QC)工作经验,现为某疫苗生产企业QA,主要负责QC的变更、偏差、OOS、OOT等质量事件的处理及其CAPA工作。
费 用&福 利
Cost & benefit
1、培训原价:1999元/人(含授课费/证书费/发票)
2月10日前:1599元/人(报2再送1)
2月10日起:1999元/人(报2再送1)
2、药视网VIP会员于优惠价(1599元)基础上享受5折(799元)参与本次学习营
3、汇款方式:
户名:徐州易云企业服务有限公司
开户行:中国工商银行徐州市淮海东路支行
账号:1106020409210313389
(付款请注明“GMP验证第六期”)
报 名 咨 询
Registration consulting
扫描识别下方二维码进行报名咨询

报名及VIP咨询
组 织 单 位
Organizational units
主办单位:药视网
承办单位:徐州易云企业服务有限公司
支持单位:药搭文档管理系统苏州豚鼠科技有限公司
支持媒体:蒲公英、药仪网、药聘网、药问问
培训对象:主要面向药品研发、生产企业的验证相关管理人员及技术人员和对验证感兴趣的其他工作人员等。
| 文件名 | 上传时间 | 大小 |
|---|